La tabla periodica es una herramienta utilizada comúnmente en la química. En ella se disponen todos los elementos químicos en una tabla (de allí su nombre). Estos se ordenan según su número atómico, que es equivalente al número de protones. En este orden le siguen la configuración de electrones y por supuesto, sus propiedades químicas.
Esta clasificación da lugar a lo que se conoce como tendencias periódicas, lo cual no es más que elementos químicos agrupados en una misma columna pues su comportamiento es similar.
Theodor Benfey, filólogo alemán, definió la tabla periódica como ‘el corazón de la química’. Llegó a compararla con la teoría de la evolución fundada por la biología y las leyes de la termodinámica establecidas por la física.
Tabla de Contenidos
Tabla periodica: resumen rápido
Para comprender un poco la tabla periodica de los elementos, es necesario saber que las filas se conocen como períodos, mientras que las columnas son grupos. Un ejemplo rápido sería: el grupo 17 pertenece a los halógenos mientras que el grupo 18 contiene a los gases nobles.
Al mismo tiempo, la tabla periódica se encuentra dividida en cuatro bloques donde los elementos se agrupan de acuerdo a ciertas propiedades químicas similares.
Gracias al orden que mantiene la tabla periódica, esta puede ser usada para encontrar relaciones entre las propiedades de los elementos. De igual manera, permite pronosticar las propiedades de nuevos elementos que aún no se han sintetizado o descubierto. A través de los años, la tabla ha sido una herramienta de suma importancia pues permite analizar el comportamiento químico de los elementos, siendo usada en muchas otras ciencias, además de la química.
Fue en 1869 cuando Dmitri Mendeléyev hizo pública la primera versión de la tabla periódica. Esta recibió un gran reconocimiento en su momento. Esta tabla fue creada para mostrar tendencias periódicas en las propiedades de los elementos conocidos para esa época. Este basamento partió de las propiedades químicas de dichos elementos.
Mendeléyev logró descubrir algunas propiedades de elementos desconocidos para su época, anticipando su ocupación dentro de los lugares vacíos de la tabla. Tiempo después se logró de mostrar, con el descubrimiento de nuevos elementos, que casi todas sus predicciones eran correctas.
Desde su descubrimiento y hasta nuestros días, la tabla periodica de los elementos ha sufrido evoluciones y ampliaciones, mejorando cada vez gracias al descubrimiento o el sintetizado de nuevos elementos. También ha permitido desarrollar modelos teóricos nuevos que explican el comportamiento químico. La estructura de la tabla periodica conocida hoy en día fue diseñada por Alfred Werner, quien tomo como base la versión de Mendeléyev.
Hasta el día de hoy han logrado descubrir o sintetizar los elementos atómicos, iniciando desde el 1 (hidrógeno) hasta el 118 (oganesón). La IUPAC recientemente confirmó los elementos 113, 115, 117 y 118, en específico, el 30 de noviembre de 2015. Estos fueron hechos públicos el 28 de noviembre de 2016. Los 94 primeros elementos de la tabla existen de forma natural. Sin embargo, algunos de ellos han sido encontrado en pequeñas cantidades, por lo que se procedió a sintetizarlos en el laboratorio antes de encontrarlos en la naturaleza.
Los elementos atómicos del 95 al 118 solo han podido se han logrado obtenerlos a través de la sintetización. En tiempos pasados, los elementos del 95 al 100 se podían encontrar en la naturaleza, pero ya no. Hasta nuestros días la investigación para descubrir nuevos elementos de números atómicos más altos sigue.
Historia tabla periodica
Para comprender la historia de la tabla periodica de los elementos, es necesario conocer primero su relación con diversos aspectos en el desarrollo de la física y la química, estos son:
- Descubrimiento de los elementos de la tabla periodica.
- Estudio de las propiedades comunes de los elementos y su clasificación.
- Noción de la masa atómica (conocida anteriormente como ‘peso atómico’). Hoy en día conocida como número atómico.
- Relación entre el número atómico y las propiedades periódicas de los elementos.
- Descubrimiento de nuevos elementos.
Descubrimiento de los elementos de la tabla periodica
Desde la antigüedad ya se conocía la existencia de algunos elementos como el cobre (Cu), mercurio (Hg), oro (Au), plata (Ag) y plomo (Pb). Sin embargo, el primer elemento químico que se descubrió a través de un proceso químico fue el fósforo (P), durante el siglo XVII, gracias al alquimista Henning Brand.
A lo largo del siglo XVII d.C. se descubrió una gran cantidad de elementos. Gracias al desarrollo de la química neumática se logró conocer los elementos más importantes: los gases, en específico: hidrógeno (H), nitrógeno (N) y oxígeno (O). Durante esos años también se asentaron las bases de la concepción de los elementos. Esta concepción llevó a Antoine Lavoisier a redactar su reconocida lista de sustancias simples, conformada por 33 elementos.
Durante los inicios del siglo XIX d.C., la implementación de la pila eléctrica dentro del estudio de fenómenos químicos permitió conocer nuevos elementos. Estos serían los metales alcalinos y alcalino-térreos. Humphry Davy fue un científico clave en esta tarea. Gracias a ello, ya para 1830 se conocían 55 elementos.
No fue sino hasta la mitad del siglo XIX d.C y gracias a la invención del espectroscopio que se pudo conocer nuevos elementos. La mayoría de ellos recibieron el nombre según el color de su línea espectral característica: cesio (Cs, del latín caesĭus, azul), rubidio (Rb, rojo), talio (Tl, de tallo, por su color verde), entre otros.
A lo largo del siglo XX d.C el estudio de los procesos radioactivos ocasionó un descubrimiento en cascada en una lista de elementos pesados (la mayoría de ellos son sustancias artificiales sintetizadas en laboratorios y su período de estabilidad es muy limitado). Gracias a ello, se pudo llegar hasta los 118 elementos con denominación aceptados por la IUPAC en noviembre de 2016.
Antecedentes de la tabla periodica
Los antecedentes de la tabla periódica se remontan a los intentos tempranos de organizar los elementos químicos. A continuación, se presentan algunos hitos importantes en el desarrollo de la tabla periódica:
Clasificación por similitudes químicas
En el siglo XVIII, varios químicos, como Johann Wolfgang Döbereiner y Alexandre-Émile Beguyer de Chancourtois, notaron que ciertos elementos exhibían propiedades químicas similares. Döbereiner agrupó elementos en tríadas basadas en similitudes químicas, mientras que Chancourtois representó los elementos en una hélice cilíndrica conocida como tornillo telúrico.
Ley de las octavas
En 1864, John Newlands propuso la ley de las octavas, donde observó que los elementos químicos exhibían similitudes cada ocho elementos cuando se organizaban según su masa atómica. Esta ley fue la primera tentativa de organizar los elementos de manera sistemática.
Clasificación periódica
En 1869, el químico ruso Dmitri Mendeléyev y el químico alemán Julius Lothar Meyer presentaron de manera independiente una versión más completa y coherente de la tabla periódica. Mendeléyev organizó los elementos conocidos hasta entonces en función de su masa atómica y las propiedades químicas, y dejó espacios vacíos para elementos aún no descubiertos. Además, Mendeléyev predijo correctamente las propiedades de los elementos aún no conocidos en esos espacios.
Descubrimiento de los gases nobles
En 1894, el químico inglés Sir William Ramsay descubrió los gases nobles (helio, neón, argón, criptón y xenón), que no encajaban en la clasificación de Mendeléyev. Los gases nobles se agregaron a la tabla periódica como un nuevo grupo.
Desarrollo de la tabla moderna
A lo largo del siglo XX, la tabla periódica se fue refinando y mejorando. Se descubrieron y sintetizaron nuevos elementos, y se reorganizaron en función de su número atómico en lugar de su masa atómica. En 1913, Henry Moseley estableció la base para la clasificación por número atómico al demostrar que las propiedades de los elementos estaban relacionadas con la carga nuclear, que a su vez está determinada por el número atómico.
Propiedades periodicas y noción de elemento
Como era de esperar, uno de los requisitos indispensables para la construcción de la tabla periódica era el descubrimiento de una cantidad asaz de elementos químicos individuales. Solo así sería posible dar con algún patrón en el comportamiento químico de los elementos y sus propiedades. Luego del primer descubrimiento, durante los dos siglos siguientes se buscó adquirir más conocimiento acerca de estas propiedades. Al mismo tiempo, también se descubrieron nuevos elementos.
Durante el siglo XVIII d.C., se conocía en la química las tablas de afinidad. Estas eran una herramienta que permitía comprender la composición química. Esta tabla de afinidad puede comprenderse mejor en el Tratado elemental de química de Lavoisier. Gracias a esta obra fue posible saber cuáles de las sustancias conocidas para ese momento eran elementos químicos, cuáles eran sus propiedades y cómo aislarlas.
Tanto el descubrimiento de los nuevos elementos químicos como el estudio de sus propiedades revelaron la existencia de ciertas similitudes entre ellos. Viendo esto, los químicos se interesaron más en un modo de clasificarlos.
Pesos atómicos de los elementos químicos
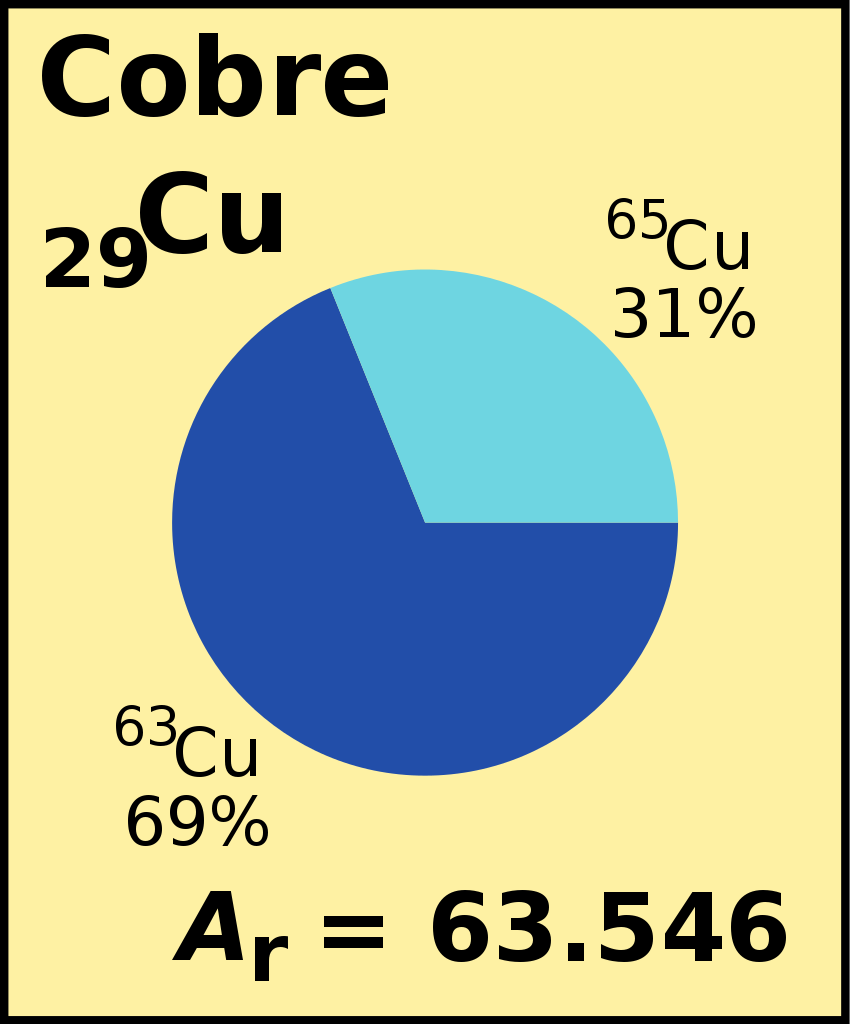
John Dalton, a inicios del siglo XIX d.C., expuso un nuevo concepto sobre el atomismo. Este surgió de sus estudios meteorológicos y sus investigaciones de los gases de la atmósfera. El principal aporte de Dalton se basa en la enunciación de un ‘atomismo químico’ que daba lugar a la posibilidad de mezclar el nuevo concepto de elemento establecido por Lavoisier y las leyes ponderales de la química.
Para ello, Dalton aplicó los conocimientos sobre proporciones a las cuales reaccionaban las sustancias químicas en su época. Con ello realizó ciertas especulaciones acerca del modo en que los átomos se fusionaban en las sustancias. Para ello, determinó la masa como unidad de referencia de un átomo de hidrógeno. El resto de los valores fueron referidos a esta unidad, lo cual le permitió crear un sistema de masas atómicas relativas.
Un ejemplo rápido sería el caso del oxígeno. Dalton inició suponiendo que el agua era un compuesto binario. Este líquido se conformaba a partir de un átomo de hidrógeno y otro de oxígeno. De momento, no tenía un método que le permitiera validar tal especulación, por lo que esta suposición terminó convirtiéndose en una posibilidad a priori.
Dalton tenía la certeza de que una parte de hidrógeno podía combinarse con siete partes (actualmente podemos afirmar que son ocho) de oxígeno para crear agua. Por ende, si tal combinación era generada átomo a átomo, es decir, un átomo de oxígeno combinándose con un átomo de hidrógeno, entonces la relación entre las masas de estos átomos sería 1:7 (actualmente es de 1:8).
Estos estudios dieron como resultado la primera tabla de masas atómicas relativas (o como los llamaba Dalton, ‘pesos atómicos’). Posteriormente, esta tabla sufrió ciertas modificaciones. Esto se debió a que ciertas imprecisiones (como la mencionada anteriormente) fueron motivo de polémicas y disparidades en cuanto a las fórmulas y los pesos atómicos. Estos comenzarían a esclarecerse en gran parta durante el congreso de Karlsruhe en 1860.
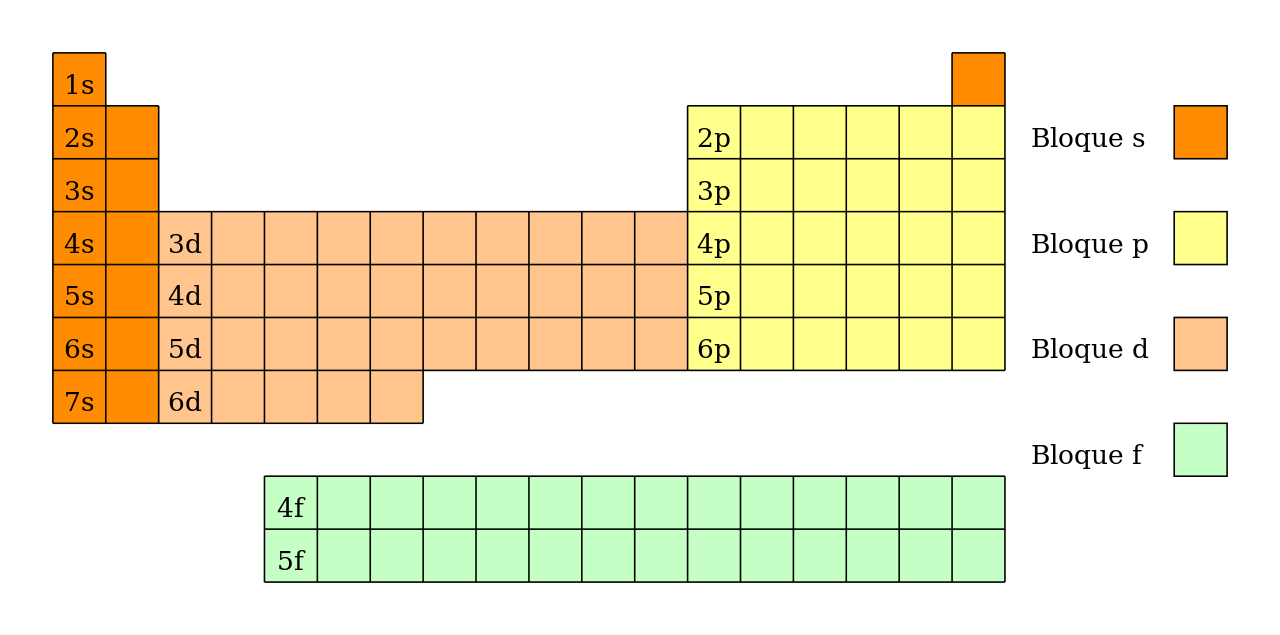
Bloques de la tabla periodica
Los bloques de la tabla periódica son los siguientes:
Bloque s de la tabla periódica
Este bloque está ubicado en la parte izquierda de la tabla periódica y comprende los grupos 1 y 2, junto con el helio (grupo 18). Los elementos en este bloque tienen sus electrones de valencia en subniveles s.
Bloque p de la tabla periódica
Este bloque se encuentra en la parte derecha de la tabla periódica y comprende los grupos 13 al 18. Los elementos en este bloque tienen sus electrones de valencia en subniveles p.
Bloque d de la tabla periódica
Este bloque se ubica en el centro de la tabla periódica, entre los bloques s y p. Comprende los grupos 3 al 12 y se conoce como la serie de transición. Los elementos en este bloque tienen sus electrones de valencia en subniveles d.
Bloque f de la tabla periódica
Este bloque se encuentra debajo de la tabla periódica y comprende los dos periodos adicionales, llamados las series de lantánidos y actínidos. Los elementos en este bloque tienen sus electrones de valencia en subniveles f.
Tanteos para la sistematización de los elementos de la tabla periódica
Tabla de Lavoisier
Antoine Lavoisier hizo público en 1789 una lista con 33 elementos químicos. Estos los agrupó en gases, metales, no metales y tierras. Si bien resulta muy práctica e incluso es aún funcional en la tabla periodica moderna, esta fue rechazada. La razón se debe a que existían muchas diferencias en las propiedades químicas y físicas.
Las tríadas de Döbereiner
Durante el siglo siguiente, los químicos trabajaron en una estructura de clasificación más precisa. Uno de los primeros tanteos para agrupar los elementos químicos según sus propiedades análogas y darles una relación con los pesos atómicos fue realizado por Johann Wolfgang Döbereiner.
En 1817 dio a conocer la gran similitud que guardaban las propiedades de unos grupos específicos de tres elementos. En ellos se podía notar una variación gradual del primero al último. Más tarde, en 1827 destacó la existencia de otros grupos donde se presentaba una relación similar: azufre, selenio y telurio; litio, potasio y sodio; bromo, cloro y yodo.
Este conglomerado de tres elementos se le llamó tríadas. Al clasificarlas, Döbereiner manifestaba que el promedio del peso atómico de los pesos de los elementos extremos, es similar al elemento del medio. Tal afirmación fue bautizada como la ley de las Tríadas.
Durante un tiempo, Leopold Gmelin, químico alemán, utilizó este sistema. Para 1843 ya había logrado identificar diez tríadas, tres grupos de cuatro elementos y un grupo compuesto por cinco elementos. En 1857 Jean-Baptiste Dumas hizo pública una investigación donde expone la relación que existe en los diferentes grupos de metales. Si bien los químicos lograron identificar la relación entre los elementos de un pequeño grupo de elementos, todavía les faltaba desarrollar un esquema que pudiera agruparlos a todos.
Ese mismo año, el químico alemán August Kekulé descubrió que el carbono tiende a unirse a otros cuatro átomos. Por ejemplo, el metano contiene un átomo de carbono y cuatro de hidrógeno. Más tarde este concepto sería conocido como ‘valencia’.
Tabla periodica espiral
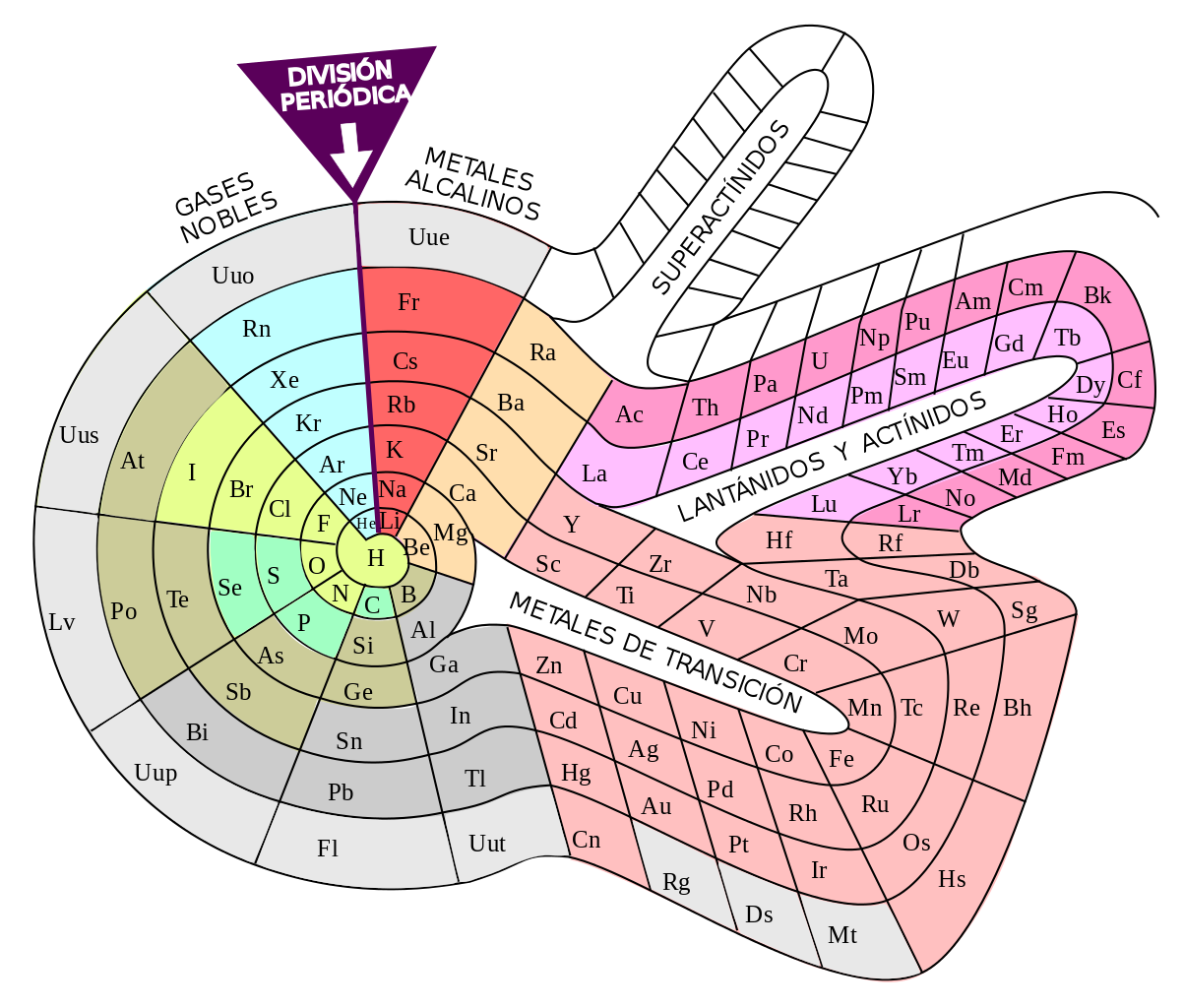
Ya en 1862 Alexandre de Chancourtois, geólogo francés publicó lo que sería una primera edición de tabla periodica de los elementos. Esta fue bautizada con el nombre de ‘hélice telúrica’ o ‘tornillo’. de Chancourtois fue el primero en descubrir que los elementos químicos tenían una periodicidad.
Esto lo demostró colocando los elementos en espiral sobre un cilindro, manteniendo un orden creciente según el peso atómico. Así, validó que los elementos con propiedades similares tienden a ocurrir en intervalos regulares. Al mismo tiempo, la tabla contenía datos sobre los iones y compuestos. También añade términos geológicos en lugar de químicos y no agrega un diagrama. Como resultado, su tabla periodica no obtuvo la atención debida hasta el trabajo de Dmitri Mendeléyev.
Primera tabla periodica con valencias
Ya para 1864 el químico alemán Julius Lothar Meyer publicó su tabla. Esta contenía 44 elementos agrupados por valencia. Con esta tabla, Meyer demostró que los elementos con propiedades similares tienden a compartir la misma valencia.
Por su parte, William Odling, químico inglés, hizo público una estructura con 57 elementos esquematizados según su peso atómico. Esta tabla presentaba algunos vacíos e irregularidades, sin embargo, notó lo que podría ser una periodicidad de pesos atómicos entre los elementos, lo cual era acorde con las ‘agrupaciones que normalmente se estructuraban’. Odling sugiere la idea de una ley periódica, pero siguió tal ley. En 1870 presentó una clasificación basada en la valencia de los elementos.
Tabla periódica de Mendeléyev
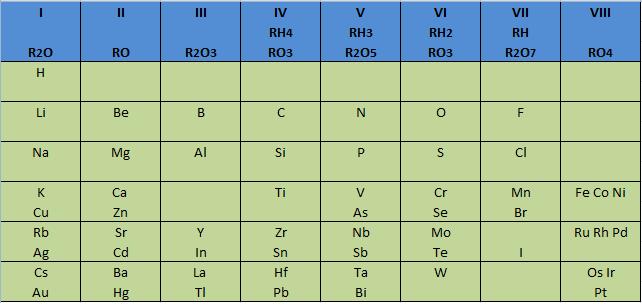
El profesor de química, Dmitri Ivánovich Mendeléyev, en 1869 publicó su primera Tabla Periodica en Alemania. Un año más tarde Julius Lothar Meyer hizo pública una versión ampliada y mejorada de su tabla publicada en 1864, basándose en la periodicidad de los volúmenes atómicos en función de la masa atómica de los elementos químicos.
Para esta época, ya se conocían 63 de los 92 elementos que existen en nuestra naturaleza, desde el Hidrógeno al Uranio. Tanto Mendeléyev como Meyer ordenaron los elementos de forma progresiva según su masa atómica.
Estos fueron agrupados en filas o períodos con de diferente longitud, situando los elementos en grupos según la similitud de sus propiedades químicas, como la valencia. Desarrollaron sus tablas creando una lista de los elementos en filas o columnas según su peso atómico y cada nueva fila o columna iniciaba cuando las características de los elementos tendían a repetirse.
Las predicciones de Mendeléyev
La tabla de Mendeléyev fue reconocida y aceptada gracias a dos decisiones que tomó el científico. En primer lugar, dejó huecos cada vez que parecía haber un elemento que todavía no había sido descubierto.
No fue el primer científico en hacerlo, pero sí en ser reconocido en el aplicar tendencias en su tabla periódica para predecir las propiedades de los elementos faltantes. Incluso, Mendeléyev llegó a pronosticar las propiedades de algunos de ellos: el germanio (Ge), que llamó eka-silicio; el galio (Ga), al que llamó eka-aluminio por encontrarse debajo del aluminio; el escandio (Sc); y el tecnecio (Tc), este último, al aislarse químicamente a partir de los restos de un sincrotrón, se convirtió en 1937 en el primer elemento producido de forma artificial.
En segundo lugar, Mendeléyev decidió ignorar el orden sugerido por peso atómico. Además, cambió los elementos adyacentes como telurio y yodo, para buscar clasificarlos según su familia química.
En 1913, Henry Moseley, estableció los valores experimentales de la carga nuclear, o también conocido como el número atómico de los elementos. Con ello comprobó que el orden de Mendeléyev efectivamente corresponde al obtenido cada vez que se aumenta el número atómico.
Estos números y su significado dentro de la organización de la tabla periódica no se apreciaron completamente hasta que se comprendió la existencia y las propiedades de los neutrones y los protones. La tabla periódica de Mendeléyev usa el peso atómico en lugar del número atómico para ordenar los elementos. Para ese momento era una información que podía determinarse con precisión.
El peso atómico funcionó muy bien en casi todos lo casos, siendo de mucha utilidad en la predicción de las propiedades de los elementos faltantes. Este método tenía una precisión mucho mayor que cualquier otro conocido para ese momento. En ese momento, Moseley predijo que los elementos faltantes entre aluminio (Z=13) y oro (Z=79) eran Z= 43, 61, 72 y 75. Estos elementos se descubrieron tiempo después. A pesar de que se han descubierto y sintetizados nuevos elementos, hoy en día todavía se utiliza la secuencia de números atómicos.
Segunda tabla periodica de Mendeléyev
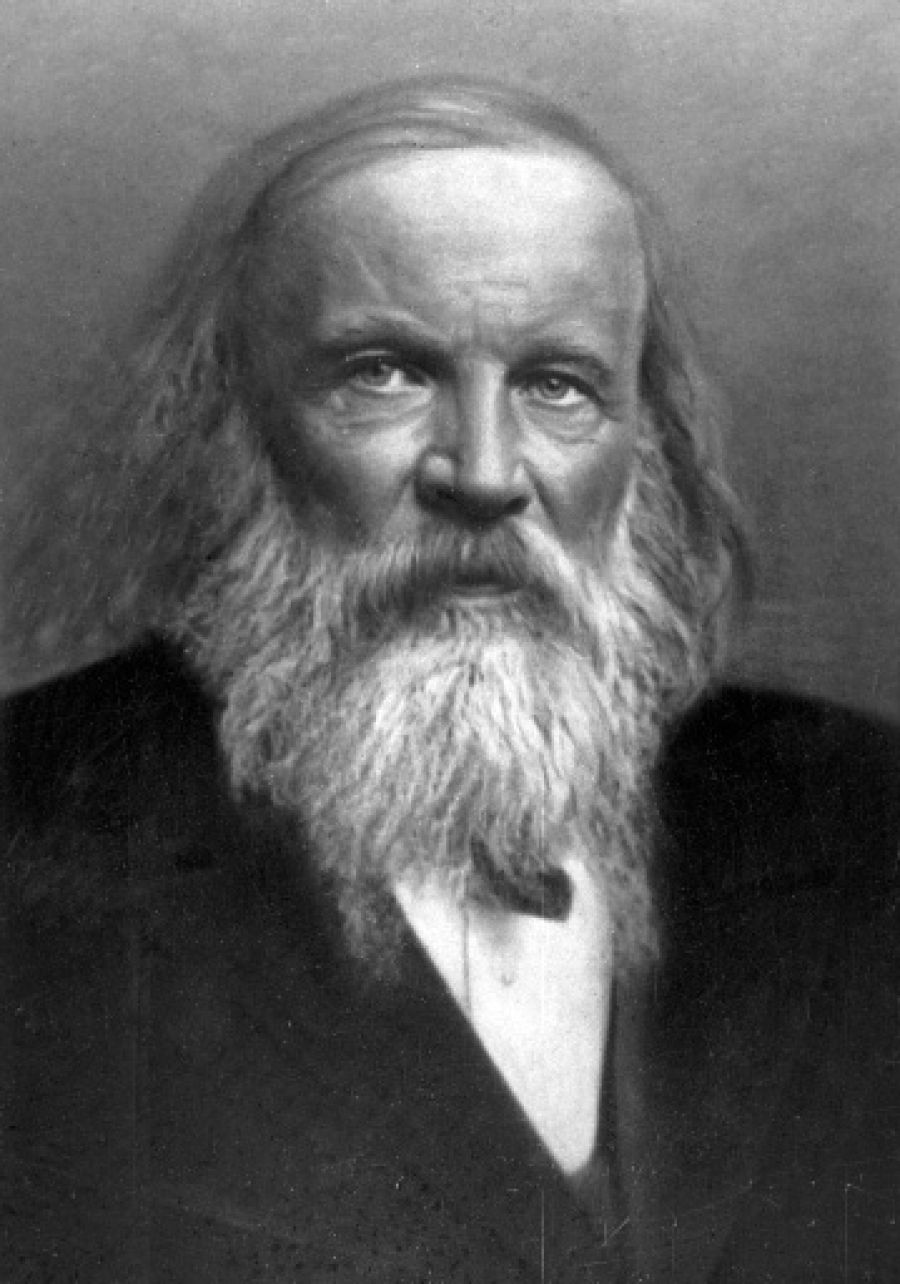
Después de presentar la primera en tabla periodica, Mendeléyev publica en 1871 una segunda tabla con ciertas mejoras. Esta tabla tiene los grupos de elementos similares dispuestos en columnas, en lugar de filas. La numeración va de I a VIII según el estado de oxidación de cada elemento.
Así mismo, realizó predicciones detalladas de las propiedades de los elementos faltantes. Estos vacíos fueron llenados tiempo después cuando los químicos descubrieran los elementos naturales adicionales.
La segunda tabla periodica de Mendeléyev mantiene un criterio de orden de columnas según los hidruros y óxidos que estos elementos puedan formar. Esto hace que implícitamente se ordenen según las valencias de los elementos.
Sin embargo, seguía obteniendo resultados contradictorios (Oro y Plata se duplican, no existen una separación entre Magnesio y Berilio con Aluminio y Boro). Pero esto marcó un gran avance.
Más tarde esta tabla fue completada con otro grupo: los gases nobles. Estos fueron descubiertos en vida por Mendeléyev, sin embargo, dadas sus características, no tenían lugar en la tabla. Transcurrieron casi 30 años, hasta 1904, para que se incorporara el grupo o valencia cero, haciendo más completa a la tabla.
Regularmente se afirma que el último elemento natural descubierto fue el francio (al cual Mendeléyev denominó eka-cesio) en 1939. No obstante, el plutonio, producido sintéticamente en 1940, logró identificarse en 1971 (luego de encontrarlo en cantidades mínimas) como un elemento de origen natural.
La estructura de la tabla periódica estándar se le atribuye a Horace Groves Deming, químico americano quien en 1923 publicó un modelo de la tabla periodica con 18 columnas. En 1928 Merck and Company creó un folleto con esta tabla, el cual fue difundido en las escuelas estadounidenses. Ya para la década de 1930, esta tabla periódica aparecía en los manuales y enciclopedias de química.
Expansión progresiva de la tabla periódica
Era de esperarse que la tabla periodica de Mendeléyev tuviese sus irregularidades. Décadas más tarde, fue necesario integrar los descubrimientos de los gases nobles, las ‘tierras raras’ y los elementos radioactivos. Otro problema presente en la tabla eran las irregularidades que se presentaban al compaginar el criterio de ordenación por peso atómico creciente y la estructura por familias con propiedades químicas comunes.
Un ejemplo de esta dificultad aparece en las parejas yodo-telurio, potasio-argón y níquel-cobalto. En estas es necesario modificar el criterio de pesos atómicos crecientes con inclinación hacia el grupo de familias con propiedades químicas similares.
Descubrimiento del número atómico
Fue necesario que pasaran unos años hasta que Henry Moseley lograr resolver este problema satisfactoriamente gracias a su estudio sobre los espectros de rayos X, publicado en 1913. Moseley demostró que se podía obtener una recta si se representaba la raíz cuadrada de la frecuencia de la radiación, en función del número de orden en el sistema periódico. Como resultado, era posible ver que no se trataba de un orden casual sino del reflejo de una propiedad de la estructura atómica. Actualmente esa propiedad se conoce como el número atómico (Z) o número de cargas positivas del núcleo.
La definición actualmente aceptada de la ley periódica aparece luego de los desarrollos teóricos elaborados durante el primer tercio del siglo XX. En específico, cuando se creó la teoría de la mecánica cuántica. Los resultados obtenidos de estos estudios y su posterior desarrollo, permitieron aceptar que la ordenación de los elementos en el sistema periódico se relaciona con la estructura electrónica de los átomos de los elementos de la tabla periodica. A partir de estos es posible predecir sus propiedades químicas.
Reforma de los actínidos y lantánidos
El científico estadounidense Glenn Seaborg sugirió en 1945 que los actínidos, al igual que los lantánidos, deberían llenar un subnivel f en lugar de una cuarta fila del bloque d, como hasta ese momento se creía. Los colegas de Seaborg le persuadieron de no publicar tan radical teoría dado que era muy probable que ésta arruinase su carrera. Sin embargo, Seaborg consideraba que su carrera no podía caer en descrédito para ese momento, por lo que decidió publicarlo. Tiempo después se demostró que tenía razón, por lo que en 1951 fue galardonado con el Premio Nobel de Química gracias a su trabajo en la síntesis de los actínidos.
Si bien algunos elementos transuránicos pueden producirse de forma natural en cantidades pequeñas, todos ellos se descubrieron por primera vez en los laboratorios. El primero de ellos fue el neptunio, siendo sintetizado en 1939. Gracias a la producción de estos elementos, la tabla periódica ha logrado expandirse significativamente.
Estos son elementos muy inestables y de caída rápida, por lo que resulta muy difícil detectarlos y caracterizarlos al realizar la sintetización. Esto ha ocasionado controversias en cuanto a la aceptación de las pretensiones y derechos de descubrimiento de ciertos elementos, lo cual exige una revisión independiente para esclarecer cuál de las partes tiene prioridad y, por ende, los derechos del nombre. El 31 de mayo de 2012 fueron nombrados el flerovio (elemento 114) y livermorio (elemento 116). Una colaboración entre Rusia y Estados Unidos en 2010, tuvo como resultado el sintetizado de seis átomos de teneso (elemento 117).
La IUPAC reconoció oficialmente el 30 de diciembre de 2015 los elementos 113, 115, 117 y 118, completando así la séptima fila de la tabla periódica. El 28 de noviembre de 2016 se hizo público los nombres oficiales y los símbolos de los últimos elementos aprobados por la IUPAC: Nh, nihonio; Mc, moscovio; Ts, teneso; y Og, oganesón.
Estructura y organización de la tabla periódica
Desde su invención hasta la actualidad la tabla periódica ha sido el sistema donde están clasificados todos los elementos químicos. Dichos elementos se enumeran de izquierda a derecha, de arriba abajo manteniendo un orden creciente por el número atómico. Cada uno de los elementos de la tabla periódica están conformados por siete filas horizontales denominadas periodos y dieciocho columnas verticales con el nombre de grupos o familias.
El número atómico y el iónico va aumentando orientándose hacia abajo y a la izquierda.
Arriba y a la derecha crece la afinidad electrónica, la electronegatividad y la energía de ionización.
Grupos de la tabla periódica
Las columnas verticales poseen el nombre de familias o grupos. Una tabla periódica estándar cuenta con dieciocho familias. En acuerdo al convenio internacional de denominaciones, las familias o grupos se enumeran del 1 al 18 empezando desde la primera columna izquierda, donde se encuentran los metales alcalinos, hasta columna final de la derecha, conformada por los gases nobles.
Anteriormente, los números romanos se definían según el último digito actual (los componentes de la cuarta familia se encontraban en el “IVB” y el decimocuarto grupo se encontraba en el “IVA”). En Estados Unidos, cada número era continuado por una letra: “A” si pertenecía al bloque S o P, y una “B” si pertenecía al D.
Europa aplicó letras al igual que Estados Unidos, con la diferencia que “A” era usado cuando el grupo precedía al 10 y “B” para el grupo 10 en adelante. Aparte de ello, los grupos 8, 9 y 10 se clasificaban como un grupo triple único, denominado popularmente en ambas numeraciones como el grupo VIII. En el año 1988 se implementó el uso del sistema de nomenclatura “IUPAC”, desechando las clasificaciones de grupo anteriores.
Varios de los grupos de la tabla periódica poseen “nombres triviales” (no metódicos) que, a pesar de que no se usan tanto. El bloque grupal del tres al diez, cuenta con nombres poco comunes, denominados de manera sencilla por el número de sus grupos o por el nombre del primer elemento del grupo, esto es a consecuencia de que dichos grupos muestran un menor parecido y/o tendencia vertical.
Composición de los grupos de la tabla periódica
La actual definición de la clasificación de la tabla periódica se basa en que los segmentos de cada grupo cuentan con arreglos electrónicos parecidos, incluso la valencia, la cual entendemos como la cantidad de electrones de la capa final. En vista de que las características dependen fuertemente de cada una de las acciones reciprocas de cada uno de los electrones que se ubican en los niveles exteriores, los elementos pertenecientes a un grupo poseen cualidades químicas en común y, a su vez, exhiben una costumbre en sus características de elevar el número atómico.
|
|
|
De este modo decimos que, los elementos de la primera familia o grupo poseen una configuración electrónica ns1 con una valencia de 1 (un solo electrón exterior), electrón que pierden al entrelazarse como un ion positivo de +1. Los elementos del último conjunto a la derecha lo conforman gases nobles, elementos cuyo elemento de energía está lleno, gracias a esto son increíblemente no reactivos; los podemos denominar también “gases inertes”.
Los componentes de una misma familia suelen manifestar esquemas en la energía de ionización, electronegatividad y el radio atómico. Desde arriba hacia abajo, de manera grupal, los radios atómicos de cada elemento van creciendo. Tomando en cuenta que existen diversas fases de energía más llenas, los electrones de valencia están más separados de su núcleo.
Desde la parte alta, sucesivamente, cada componente posee una energía de ionización inferior, debido a que es más sencillo remover un electrón de los átomos que están más débilmente unidos. De igual manera, un conjunto posee un decrecimiento de electronegatividad desde el área superior hasta la inferior a causa de un intervalo que aumenta cada vez más entre el núcleo y los electrones de valencia.
Entre estos estándares existen excepciones, tal como en el grupo 11: la electronegatividad crece más en la parte inferior del grupo. Asimismo, en algunas zonas de la tabla periódica, como el conjunto de bloques F y D las semejanzas horizontales podrían estar o ser más acentuadas que los mismos verticales.
Períodos de la tabla periodica
Períodos se denominan todas aquellas filas horizontales de la tabla periódica. La proporción de niveles energéticos de un átomo define el período al que corresponde. Cada nivel o etapa está dividida en subniveles diferentes que, a medida que el número atómico crece, se desarrolla el siguiente orden:
Los elementos dentro de un mismo período manifiestan capacidades parecidas en afinidad electrónica, energía de ionización, electronegatividad y radio atómico. En un período, el radio atómico suele disminuir al desplazarse a la derecha a causa de que cada componente periódico agregó electrones y protones, provocando que los electrones se arrastren sucesivamente aproximándose más al núcleo.Guiándonos por esa regla, cada uno de los elementos se ubica en función a su configuración electrónica para darle sentido a la tabla periódica.
La reducción del radio atómico provoca a su vez, que la electronegatividad y la energía de ionización crezcan de izquierda a derecha en un período, esto se debe a que el núcleo atrae los electrones. La semejanza electrónica presenta también una ligera predisposición a lo ancho de cada período. Los metales (ubicados en la izquierda) normalmente poseen una menor afinidad que el grupo de no metales (ubicados a la derecha del período), sin embargo, ocurre una excepción con los gases nobles.
Bloques de la tabla periódica
Podemos dividir la tabla periódica en bloques en sucesión a la forma que se vayan llenando las capas de electrones de cada elemento. Cada bloque se define en base al orbital en el que mora (teóricamente) el electrón final: S, D, P y F.
Bloque S
Está conformado por las dos primeras familias o grupos, grupos de alcalinotérreos y metales alcalinos, tales como el helio y el hidrógeno.
Bloque D
Lo conforma los grupos del 3 al 12, en el se encuentran los metales de transición.
Bloque P
Compuesto por los seis últimos grupos, grupos que van del 13 al grupo 18, el bloque P están principalmente los metaloides, entre diversos elementos.
Bloque F
Comúnmente ubicado al final de la tabla periódica, no cuenta con numeración grupal, está compuesto por actínidos y lantánidos.
Metales, metaloides y no metales de la tabla periódica
En relación con las características químicas y físicas compartidas, cada elemento se puede clasificar entre tres clases: metales, metaloides y no metales. Normalmente, los metales, firmes y brillantes, son de los conductores más poderosos, capaces de establecer fusiones entre sí y con diversos compuestos iónicos equivalentes a sales con agregados no metálicos (menos los gases nobles).
Por lo general, los no metales son gases coloridos o sin color; se pueden formar vínculos covalentes junto con diversos componentes no metálicos. Entre metales y no metales tenemos aquellos que poseen características mixtas o intermedias, denominados como metaloides.
Clasificación de los metales en la tabla periódica
Los metales y no metales se pueden clasificar por subclases que demuestren la progresión desde lo metálico hasta las características no metálicas, partiendo de izquierda a derecha, en sus filas: metales alcalinos, de alta reactividad; metales menos reactivos, como los alcalinotérreos; actínidos metales de transición y lantánidos, metales de post – transición.
Los del grupo de no metales se subclasifican de manera sencilla en no metales poliatómicos, metales que, al estar más próximos a los metaloides presentan un carácter metálico inicial, no obstante, los no metales diatómicos, metales no metálicos y gases nobles, elementos monoatómicos no metálicos que a su vez son casi inactivos en su totalidad. En algunos casos, se marcan subgrupos internamente en los metales de transición, como en los metales nobles y refractarios.
La clasificación de los elementos en cada una de sus clases y subclases en relación a las características que comparten resulta inexacta. Hay una galería de propiedades y características en cada clase, fácilmente se encuentran similitudes en los límites, tal como ocurre en la mayor parte de los sistemas de clasificación.
Como ejemplo, podemos hablar del berilio, denominado como un metal alcalinotérreo, a pesar que su estructura química anfótera más su orientación a desarrollar componentes covalentes, ambos son cualidades de un metal de transición químicamente frágil.
El radón, clasificado como un “no metal” y un gas noble a la vez (a pesar de poseer cualidades químicas catiónicas propias de un metal). Asimismo, podemos clasificar basándonos en la clasificación de los elementos. Este método nos lleva a finales de 1860, donde Hinrichs marcó la posibilidad de extracción de líneas de limites sencillas para manifestar los componentes que poseen características semejantes, así como elementos gaseosos, o los metales y no metales.
Valencias de la tabla periodica
Las valencias de la tabla periodica indican el número de electrones que faltan en un elemento químico o que este debe ceder para alcanzar su último nivel de energía. Estos electrones son los que juegan un papel fundamental durante una reacción química o al crear un enlace químico con otro elemento. Hay elementos de la tabla periodica con más de una valencia. Esta es la razón por el que este concepto fue reemplazado por el número de oxidación, que al final es la misma representación.
A lo largo del siglo XX, la definición de valencia ha tenido una amplia evolución, alcanzando un rango de aproximaciones para describir el enlace químico. Entre ellas está la estructura de Lewis (1916), la teoría del enlace de valencia (1927), la teoría de los orbitales moleculares (1928), la teoría de repulsión de pares electrónicos de la capa de valencia (1958) y todos los métodos de química cuántica avanzada. En la mayoría de los elementos la valencia se determina según el fluoruro más alto conocido.
Tipos de valencia
Valencia positiva máxima
Este es un número positivo que muestra la capacidad máxima de combinación que posee un átomo. Este número siempre coincide con el grupo de la tabla periodica al que pertenece.
Valencia negativa solo para el grupo A
Es un valor negativo que muestra la suficiencia de un átomo para fusionarse con otro siempre que éste se mantenga con una valencia positiva. Para determinar este valor negativo, solo hace falta contar lo que falta a la valencia positiva para alcanzar el valor 8, pero con signo negativo.
Número de enlaces
Al principio se tenía la creencia de que el número de enlaces formados por un elemento específico era una propiedad química fija. En efecto, esta suele ser una buena aproximación en muchos casos. Por ejemplo, en muchos de los compuestos, el hidrógeno forma un enlace, el oxígeno dos y el carbono cuatro. Sin embargo, poco tiempo después se descubrió que la valencia podía tener diversas variaciones entre los compuestos para muchos de los elementos.
Uno de los primeros elementos en comprobar tal afirmación fue el fósforo. Este elemento tiende a comportarse como si su valencia fuese de tres, mientras que otras veces como si fuese una valencia de cinco. Uno de los métodos para resolver este problema consiste en determinar la valencia para cada compuesto individual. Si bien elimina gran parte de la generalidad del concepto, da lugar a la idea del número de oxidación.
Por otra parte, puedes visitar ahora Fluyezcambios.
Como aprenderse la tabla periodica
Al ver la tabla periodica de los elementos podrás notar que esta contiene muchos valores complejos, que a simple vista parecen muy difíciles de aprender. Sin embargo, resulta mucho más sencillo de lo que imaginas. Para ello puedes memorizarla de forma simple o a profundidad.
Tabla periodica metales no metales y metaloides
La tabla periódica está compuesta por diferentes bloques que se organizan de acuerdo a las características de los elementos químicos. Los bloques principales de la tabla periódica son:
- Bloque s: Este bloque está ubicado en la parte izquierda de la tabla periódica y comprende los grupos 1 y 2, junto con el helio (grupo 18). Los elementos en este bloque tienen sus electrones de valencia en subniveles s.
- Bloque p: Este bloque se encuentra en la parte derecha de la tabla periódica y comprende los grupos 13 al 18. Los elementos en este bloque tienen sus electrones de valencia en subniveles p.
- Bloque d: Este bloque se ubica en el centro de la tabla periódica, entre los bloques s y p. Comprende los grupos 3 al 12 y se conoce como la serie de transición. Los elementos en este bloque tienen sus electrones de valencia en subniveles d.
- Bloque f: Este bloque se encuentra debajo de la tabla periódica y comprende los dos periodos adicionales, llamados las series de lantánidos y actínidos. Los elementos en este bloque tienen sus electrones de valencia en subniveles f.
Cabe mencionar que algunos bloques pueden subdividirse aún más en subbloques más específicos. Por ejemplo, el bloque d puede dividirse en bloques d1, d2, d3, etc., dependiendo de la configuración electrónica específica de los elementos en ese bloque.
Es importante destacar que la tabla periódica tiene múltiples formas de representación, pero los bloques mencionados anteriormente son una clasificación comúnmente utilizada para organizar los elementos químicos.
Tabla periodica metales no metales y metaloides
En la tabla periódica, los elementos químicos se pueden clasificar en tres categorías principales: metales, no metales y metaloides. A continuación se describe cada una de estas categorías:
- Metales. Los metales se encuentran en la mayoría de las áreas de la tabla periódica, especialmente en los bloques s y d. Son generalmente sólidos (excepto el mercurio, Hg), brillantes y buenos conductores de calor y electricidad. Los metales también son maleables y dúctiles, lo que significa que pueden ser martillados en láminas delgadas o estirados en alambres sin romperse. Algunos ejemplos de metales comunes incluyen el hierro (Fe), el cobre (Cu), el aluminio (Al) y el oro (Au).
- No metales. Los no metales se encuentran en el lado derecho de la tabla periódica, principalmente en el bloque p. Tienen propiedades opuestas a los metales. Por lo general, son gases o sólidos frágiles en condiciones normales, y pocos son líquidos. Los no metales tienen baja conductividad eléctrica y térmica. Además, suelen tener puntos de fusión y ebullición más bajos que los metales. Algunos ejemplos de no metales incluyen el oxígeno (O), el carbono (C), el nitrógeno (N) y el azufre (S).
- Metaloides. Los metaloides, también conocidos como semimetales, son elementos que se encuentran en la franja diagonal entre los metales y los no metales en la tabla periódica. Tienen propiedades intermedias y comparten características tanto de los metales como de los no metales. Los metaloides exhiben una combinación de conductividad eléctrica y térmica en diferentes condiciones. Algunos ejemplos de metaloides son el silicio (Si), el germanio (Ge), el arsénico (As) y el antimonio (Sb).
Memorización simple de la tabla periódica
Aprenderse la tabla periodica rápidamente es muy sencillo. Solo necesitas aplicar el sistema mayor para enlazar el número atómico con el nombre del elemento.
Por ejemplo, si deseas enlazar 1 con Hidrógeno, deberás usar la palabra en el sistema mayor asociado al número uno. Si la palabra es ‘tea’, lo único que debes hacer es crear una frase con ´Hidrógeno’.
Para 11 con Sodio (Natrium), puedes utilizar ‘dedo’ para el 11 y nariz para sodio (pues guarda similitud con Natrium).
Memorización profunda de la tabla periódica
Siguiendo el sistema anterior de memorización de la tabla periodica de los elementos, puedes agregarle otros datos para recordar más información. Estos pueden ser:
- Peso atómico
- Símbolo químico
- Punto de fusión
- Punto de ebullición
- Nombre original
- Ácido/Base
- Densidad
Otros métodos de memorización de la tabla periódica
Crea mapas mentales
Usando esta herramienta, coloca la tabla periodica como nodo principal. En el primer nivel del mapa ubica los diferentes grupos: Gases nobles, metales, entre otros. Luego, coloca en el segundo nivel los elementos de cada grupo y cada elemento agrega un nivel con sus datos. Esto también puedes hacerlo trabajando en lugar de grupos, con las filas de la tabla periodica.
Usando matrices
Crea una matriz 18×7 donde puedas guardar los elementos, excluyendo los actínidos y los lantánidos. Aparte, haz una columna 15×2 para actínidos y lantánidos. Utiliza colores para diferenciar los grupos. Las columnas puedes enumerarlas y las filas asignarles una letra.
Otros métodos para memorizar la tabla periódica serían el método de Loci o el Sistema Dominic.
Tabla periódica interactiva
Si quieres conocer los datos específicos de cada elemento de la tabla periódica, usar una tabla periodica interactiva te resultará de mucha utilidad. La tabla que te mostramos en el video a continuación, te será de mucha ayuda en al momento de estudiar y memorizar los elementos y sus datos.